
O segredo milenar do Egito que revolucionou a nossa medicina
De pão mofado a pílulas que salvam vidas, a saga dos antibióticos é mais antiga e surpreendente do que você imagina.
A chegada dos antibióticos ao mundo da medicina foi, sem exageros, o maior salto de qualidade do século XX. Essas substâncias se tornaram nossas principais aliadas para tratar e até prevenir uma infinidade de infecções bacterianas. De problemas graves como meningite até a presença de bactérias no sangue, eles estão lá para nos proteger.
No entanto, muita gente ainda confunde sua real utilidade, acreditando que eles são uma solução para qualquer mal-estar. É fundamental entender que eles são específicos para combater bactérias, e não outros tipos de micro-organismos. Mas afinal, como essas pequenas maravilhas da ciência realmente funcionam?
A história por trás desses medicamentos é uma verdadeira viagem no tempo, com raízes que nos levam até o Egito Antigo. Acredite, muito antes da medicina moderna, nossos ancestrais já tinham suas próprias versões de antibióticos. Prepare-se para descobrir uma jornada fascinante que mudou para sempre a nossa luta contra as doenças.
As origens surpreendentes dos antibióticos

Você provavelmente imagina que os antibióticos são uma invenção recente, mas a verdade é que eles são muito mais antigos do que pensamos. A busca por curas para infecções remonta a civilizações milenares que já entendiam, de forma intuitiva, o poder de certos elementos naturais. Essa sabedoria ancestral foi a semente para a revolução médica que viria séculos depois.
A prova disso está em um dos documentos médicos mais antigos que sobreviveram ao tempo, o Papiro Ebers, datado de 1550 a.C. Esse incrível tratado egípcio de conhecimento fitoterápico já listava uma série de remédios e tratamentos inovadores para a época. Entre as receitas, uma chama a atenção por sua genialidade e simplicidade: o uso de solo medicinal.
Isso mesmo, os egípcios aplicavam terra com propriedades curativas em feridas para combater infecções, uma prática rudimentar que continha a essência do que faz um antibiótico. Eles observaram que certos tipos de solo e mofo poderiam ajudar na cicatrização, iniciando uma longa tradição de combate às bactérias. Mal sabiam eles que estavam dando os primeiros passos de uma jornada que transformaria a humanidade.
Os primeiros passos no tratamento de infecções

A sabedoria para tratar infecções não era exclusividade dos egípcios, pois os gregos antigos também deixaram sua marca na história da medicina. Registros históricos mostram que eles eram mestres em observar a natureza e aplicar seus aprendizados de forma prática. Eles selecionavam cuidadosamente mofos e plantas específicas para tratar diferentes tipos de feridas e doenças.
Essa metodologia, embora baseada na tentativa e erro, demonstrava uma compreensão notável sobre as propriedades curativas do ambiente. Eles percebiam que nem todo mofo era igual e que certas plantas tinham o poder de acelerar a recuperação e evitar complicações. Era a ciência nascendo de forma orgânica, a partir da pura observação dos ciclos da vida.
Essa prática estabeleceu as bases para uma abordagem mais sistemática no combate às infecções, influenciando gerações futuras de médicos e curandeiros. O conhecimento grego se espalhou pelo mundo antigo, provando que a humanidade sempre esteve em uma busca incansável por maneiras de superar as doenças. Cada descoberta, por menor que parecesse, era um degrau a mais nessa escalada pela sobrevivência.
Hipócrates: O pai da medicina e seus métodos

Quando falamos de medicina, é impossível não mencionar Hipócrates, o médico grego que ficou conhecido como o “pai da medicina”. Ele não apenas organizou o conhecimento médico de sua época, mas também introduziu métodos que são reverenciados até hoje. Sua abordagem era focada em observar o paciente e buscar soluções lógicas para os problemas de saúde.
No tratamento de feridas infectadas, Hipócrates era um verdadeiro especialista, utilizando rotineiramente agentes com claras propriedades antimicrobianas. Ele aplicava substâncias como a mirra e diversos sais inorgânicos para limpar e proteger os ferimentos, evitando que as infecções se espalhassem. Essas técnicas eram surpreendentemente eficazes e mostravam uma profunda compreensão da necessidade de assepsia.
Seus métodos representaram um avanço gigantesco em relação às práticas puramente místicas, trazendo a razão para o centro do tratamento. Ao sistematizar o uso desses compostos, Hipócrates deu um passo fundamental na direção da medicina baseada em evidências. Ele provou que a cura poderia ser encontrada na natureza, desde que aplicada com conhecimento e cuidado.
A sabedoria egípcia e o pão mofado

Voltando ao Egito, a criatividade dos antigos para lidar com problemas de saúde parecia não ter limites. Além do solo medicinal, eles desenvolveram outra técnica surpreendente para tratar feridas infectadas. Eles aplicavam pão mofado diretamente sobre os ferimentos, uma prática que soa estranha, mas que tinha uma lógica poderosa por trás.
Esse método, combinado com o uso de vários outros materiais vegetais, era uma forma primitiva de antibioticoterapia. O mofo presente no pão, em muitos casos, era do gênero *Penicillium*, o mesmo fungo que originou a penicilina milênios depois. Sem saber, os egípcios estavam aproveitando os poderes de um dos antibióticos naturais mais potentes do planeta.
Essa prática mostra como a observação atenta da natureza pode levar a descobertas revolucionárias, mesmo sem o aparato tecnológico que temos hoje. Eles notaram que aquele pão “estragado” tinha a capacidade de limpar feridas e acelerar a cura de uma forma quase mágica. Era a prova de que as soluções para grandes problemas podem estar nos lugares mais inesperados.
A medicina popular na Idade Média

Avançando no tempo, chegamos à Idade Média, um período em que grande parte do conhecimento científico antigo se perdeu ou foi suprimido. Durante essa era, os tratamentos para infecções eram baseados principalmente no folclore medicinal. As receitas passavam de geração em geração, misturando sabedoria popular, superstição e um pouco de sorte.
Os resultados dessas práticas variavam de forma drástica, sendo muitas vezes uma verdadeira loteria para o paciente. Enquanto alguns remédios à base de ervas poderiam ter efeitos positivos, muitos outros eram completamente ineficazes ou até perigosos. A falta de um método científico fazia com que a cura dependesse mais da sorte do que do conhecimento.
Apesar da imprevisibilidade, o folclore medicinal manteve viva a ideia de que a natureza guardava segredos para a cura. Foi um período de transição, onde a sabedoria empírica lutava para sobreviver em um mundo dominado pela fé e pela tradição. Essa fase, no entanto, preparou o terreno para a redescoberta da ciência que viria nos séculos seguintes.
O primeiro uso clínico documentado de um antibiótico

O final do século XIX marcou um momento decisivo na história dos antibióticos, com o primeiro uso clínico formalmente relatado. Na década de 1890, os bacteriologistas alemães Rudolph Emmerich e Oscar Löw fizeram uma descoberta ousada. Eles decidiram usar uma bactéria para combater outra, um conceito revolucionário para a época.
Os dois cientistas utilizaram um extrato da bactéria *Pseudomonas aeruginosa* para tratar centenas de pacientes em diversos hospitais. Naquele tempo, essa bactéria era conhecida como *Bacillus pycyaneus* e seu extrato mostrou-se eficaz contra outras infecções. Foi um dos primeiros exemplos de antibioticoterapia planejada e aplicada em larga escala.
Embora essa bactéria gram-negativa específica não seja mais usada para essa finalidade hoje, a experiência abriu uma porta importante. Emmerich e Löw provaram que era possível manipular o mundo microbiano para curar doenças humanas. Eles plantaram a semente para a era moderna dos antibióticos, mesmo que seus nomes não sejam tão famosos quanto os de seus sucessores.
Os pioneiros da era moderna dos antibióticos

A transição para o século XX trouxe consigo figuras geniais que transformariam a medicina para sempre, e uma delas foi o médico alemão Paul Ehrlich. Ele é considerado um dos grandes pioneiros no desenvolvimento dos antibióticos modernos, graças à sua busca incansável pela “bala mágica”. Ehrlich sonhava com um composto que pudesse matar o agente infeccioso sem prejudicar o paciente.
Em 1909, após testar centenas de compostos, ele finalmente encontrou o que procurava ao descobrir a arsfenamina. Comercializado com o nome de Salvarsan, este foi o primeiro tratamento medicinal verdadeiramente eficaz para a sífilis. A descoberta foi um marco histórico, oferecendo esperança para uma doença que até então era uma sentença de sofrimento e morte.
O sucesso do Salvarsan provou que a quimioterapia seletiva era possível e abriu caminho para uma nova era de pesquisa farmacêutica. A “bala mágica” de Ehrlich não era perfeita, mas sua visão e persistência inspiraram uma geração de cientistas. A medicina nunca mais seria a mesma depois de sua contribuição monumental.
A revolução da penicilina com Alexander Fleming

O próximo grande salto na história dos antibióticos veio de uma descoberta que mistura genialidade e um pouco de sorte. Em 1928, o médico e microbiologista escocês Alexander Fleming notou algo estranho em seu laboratório. Uma de suas culturas de bactérias havia sido contaminada por um mofo, e ao redor desse mofo, as bactérias simplesmente não conseguiam crescer.
Fleming ficou fascinado por esse fenômeno e decidiu investigar o “suco de mofo” que estava matando as bactérias. Ele identificou o fungo como sendo do gênero *Penicillium* e batizou a substância ativa de penicilina. Nascia ali o primeiro antibiótico natural amplamente eficaz do mundo, uma descoberta que mudaria o destino da humanidade.
Embora Fleming tenha feito a descoberta inicial, foram necessários outros cientistas para purificar e produzir a penicilina em massa anos depois. Ainda assim, seu olhar atento para um acidente de laboratório deu início a uma verdadeira revolução. A penicilina se tornaria a arma secreta dos Aliados na Segunda Guerra Mundial e salvaria incontáveis vidas desde então.
A expansão da pesquisa com Selman Waksman

Seguindo os passos de Fleming, outro cientista genial levou a pesquisa de antibióticos a um novo patamar. O bioquímico e microbiologista judeu-ucraniano Selman Waksman dedicou sua carreira a estudar os micro-organismos do solo. Ele acreditava que a terra guardava um arsenal de compostos capazes de combater infecções.
Sua pesquisa sobre a decomposição de organismos que vivem no solo foi extremamente frutífera, culminando na descoberta da estreptomicina no final da década de 1930. Este novo antibiótico provou ser eficaz contra a tuberculose, uma doença que até então era praticamente incurável. A descoberta rendeu a Waksman o Prêmio Nobel e consolidou a importância de se investigar o solo em busca de novos medicamentos.
O trabalho de Waksman não parou por aí, pois ele e sua equipe descobriram vários outros antibióticos importantes. Ele cunhou o próprio termo “antibiótico” e abriu as portas para a exploração sistemática de micróbios do solo. Sua contribuição foi fundamental para o início do que viria a ser a “era de ouro” dos antibióticos.
A “era de ouro” da descoberta de antibióticos

As décadas que se seguiram à Segunda Guerra Mundial foram um período de otimismo e progresso científico sem precedentes. O final dos anos 1940 e as décadas de 50 e 60 são considerados a “era de ouro” da pesquisa e desenvolvimento de antibióticos. Foi uma época de descobertas rápidas e impactantes que transformaram o arsenal médico.
Durante essas duas décadas, uma enxurrada de novos medicamentos chegou às clínicas e farmácias de todo o mundo. Os cientistas exploraram produtos naturais de actinomicetos, fungos e outras bactérias, além de desenvolverem antibióticos totalmente sintéticos em laboratório. A cada ano, parecia haver uma nova arma para combater mais um tipo de infecção.
Essa explosão de inovação mudou radicalmente a prática médica, tornando cirurgias mais seguras e tratando doenças que antes eram fatais. A expectativa de vida aumentou e a humanidade sentiu que finalmente estava ganhando a guerra contra as bactérias. Essa era dourada deixou um legado de medicamentos que usamos até hoje e um sentimento de que a ciência poderia superar qualquer desafio.
Afinal, o que são os antibióticos?

Depois de toda essa jornada histórica, vamos ao ponto principal: o que exatamente são os antibióticos? De forma simples, eles são medicamentos poderosos projetados especificamente para tratar infecções causadas por bactérias. Sua missão é clara e direta: neutralizar esses invasores microscópicos que nos causam doenças.
Eles conseguem fazer isso de duas maneiras principais, dependendo do tipo de antibiótico. Alguns agem como verdadeiros exterminadores, destruindo as bactérias completamente e eliminando a ameaça de vez. Outros funcionam de uma maneira mais sutil, impedindo que as bactérias se reproduzam e se espalhem pelo corpo.
Em ambos os casos, o resultado é o mesmo: o sistema imunológico ganha o tempo e a ajuda de que precisa para controlar a infecção. É uma parceria poderosa entre a ciência e as defesas naturais do nosso corpo. Entender essa função é o primeiro passo para usar esses medicamentos de forma correta e responsável.
A origem natural dos antibióticos

Muitos dos antibióticos mais eficazes que temos hoje vieram diretamente da natureza, em uma verdadeira guerra microscópica. Eles são produzidos naturalmente por bactérias e fungos do solo como uma arma de sobrevivência. Em um ambiente competitivo, esses micro-organismos precisam lutar por comida, água e espaço.
Ao produzir uma substância antibiótica, um micróbio ganha uma vantagem estratégica fundamental sobre seus concorrentes. Ele basicamente elimina a competição, garantindo para si os recursos limitados daquele habitat específico. É a mais pura seleção natural acontecendo em uma escala que não podemos ver a olho nu.
A penicilina, por exemplo, é o exemplo clássico dessa estratégia, sendo produzida por um fungo para se defender de bactérias. A genialidade da ciência foi observar essa batalha, isolar a “arma” e usá-la a nosso favor. Nós pegamos emprestado o arsenal da natureza para proteger nossa própria saúde.
Como os antibióticos são produzidos em massa?
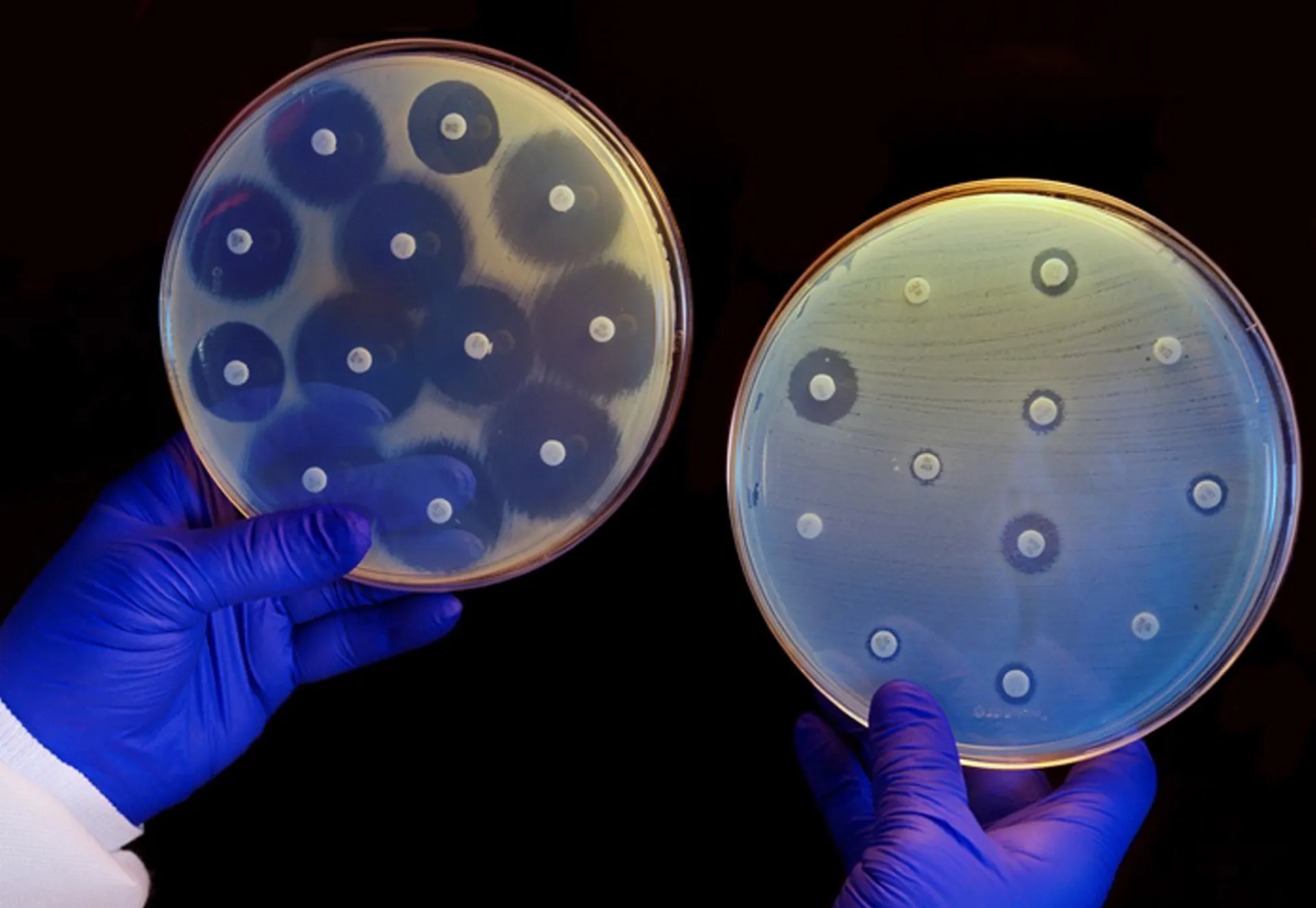
Transformar uma descoberta de laboratório em um medicamento disponível para milhões de pessoas é um desafio gigantesco. A resposta para a produção em massa de antibióticos está em um processo chamado fermentação. A microbiologia industrial usa essa técnica para cultivar os micro-organismos produtores em condições controladas.
Basicamente, o micro-organismo fonte é colocado em enormes recipientes, como tanques gigantes, que contêm um meio de crescimento líquido. Esse “caldo” nutritivo oferece tudo o que o fungo ou a bactéria precisa para se multiplicar e produzir o antibiótico desejado. É como criar uma fazenda de micróbios com um propósito muito específico.
Após o período de fermentação, o antibiótico é extraído, purificado e transformado na pílula ou injeção que chega até nós. É um processo complexo que combina biologia e engenharia para garantir a produção de medicamentos seguros e eficazes. Graças a essa tecnologia, podemos ter acesso a essas substâncias que salvam vidas.
O momento certo para usar antibióticos
Nosso corpo é equipado com um sistema de defesa incrível, o sistema imunológico, que normalmente dá conta do recado. Ele é capaz de identificar e destruir bactérias nocivas antes que elas causem grandes problemas. Na maioria das vezes, nem percebemos essa batalha silenciosa acontecendo dentro de nós.
No entanto, há momentos em que o número de bactérias invasoras é simplesmente excessivo, sobrecarregando nossas defesas. É como um exército tentando lutar contra uma força muito superior em número. É exatamente nessas horas que os antibióticos mostram o seu verdadeiro valor e se tornam essenciais.
Eles funcionam como um reforço crucial, ajudando a equilibrar a balança e dando ao nosso sistema imunológico a chance de se reorganizar e vencer a guerra. Eles não substituem nossas defesas, mas trabalham em conjunto com elas. Saber quando essa ajuda é necessária é uma decisão que deve ser sempre guiada por um profissional de saúde.
A mecânica de ação dos antibióticos
Apesar de terem o mesmo objetivo final, existem diferentes tipos de antibióticos que funcionam de maneiras distintas. Cada classe de antibiótico tem como alvo um processo vital específico dentro da célula bacteriana. Essa precisão é o que os torna tão eficazes e, ao mesmo tempo, relativamente seguros para as nossas próprias células.
Eles funcionam como chaves que se encaixam em fechaduras muito específicas da maquinaria bacteriana. Alguns interferem na capacidade da bactéria de construir sua parede celular, fazendo com que ela se rompa e morra. Outros bloqueiam a produção de proteínas essenciais, impedindo que a bactéria funcione ou se multiplique.
Essa diversidade de mecanismos de ação é fundamental, pois permite que os médicos escolham o antibiótico mais adequado para cada tipo de infecção. É uma estratégia de ataque multifacetada contra um inimigo que está sempre evoluindo. A ciência por trás de como eles funcionam é um campo fascinante e em constante desenvolvimento.
Antibióticos bactericidas: O ataque fatal

Dentro do arsenal de antibióticos, existem aqueles com uma abordagem mais agressiva, conhecidos como bactericidas. O nome já diz tudo: a missão deles é matar as bactérias de forma direta e definitiva. Eles não dão chance para o inimigo se reagrupar ou se adaptar.
A penicilina é um exemplo perfeito de um antibiótico bactericida, atacando um ponto fraco crucial da bactéria. Ela interfere diretamente na formação da parede celular bacteriana, uma estrutura essencial para a sobrevivência do micro-organismo. Sem essa parede protetora, a bactéria fica vulnerável e acaba se desintegrando.
Essa ação letal é ideal para infecções graves, onde é preciso eliminar a ameaça o mais rápido possível. Outros bactericidas podem atacar o material genético ou o conteúdo celular da bactéria, sempre com o objetivo de causar danos irreparáveis. É a força bruta da medicina agindo para nos proteger.
Antibióticos bacteriostáticos: Contendo o avanço
Em contraste com os bactericidas, temos os antibióticos bacteriostáticos, que adotam uma estratégia diferente. Em vez de matar as bactérias diretamente, eles impedem que elas se multipliquem. Eles basicamente apertam o botão de “pausa” no ciclo de vida das bactérias.
Essa tática é extremamente inteligente, pois ao frear a proliferação, eles evitam que a infecção se espalhe e se agrave. Isso dá ao nosso sistema imunológico uma vantagem enorme, pois ele pode lidar com um número estável de inimigos. É um trabalho em equipe entre o medicamento e as defesas do nosso corpo.
Os antibióticos bacteriostáticos são frequentemente usados em infecções menos agudas ou em pacientes cujo sistema imunológico está funcionando bem. Eles controlam a situação e deixam que o corpo finalize o trabalho de eliminação. É uma abordagem mais sutil, mas igualmente eficaz para restaurar a saúde.
Quando os antibióticos não são a solução

Um dos maiores equívocos sobre os antibióticos é pensar que eles servem para curar qualquer tipo de doença infecciosa. A verdade é que eles têm um alvo muito específico: as bactérias. Eles são completamente ineficazes contra infecções virais, como resfriados e gripes.
Isso acontece porque vírus e bactérias são organismos completamente diferentes, com estruturas e modos de vida distintos. Os mecanismos de ação dos antibióticos simplesmente não afetam os vírus, que se replicam dentro de nossas próprias células. Usar um antibiótico para uma gripe é como usar a chave errada em uma fechadura, simplesmente não funciona.
Essa confusão leva ao uso indevido de medicamentos, o que não só deixa de tratar a doença real como também pode trazer consequências negativas. O mesmo vale para a maioria das tosses e dores de garganta, que em grande parte são causadas por vírus. Entender essa diferença é fundamental para a nossa saúde e para a saúde de toda a comunidade.
Infecções onde eles são ineficazes

A prática médica moderna evoluiu muito e hoje entende-se melhor quando os antibióticos são realmente necessários. Por isso, eles não são mais usados rotineiramente para tratar uma série de condições comuns. Um exemplo clássico são as infecções de ouvido em crianças, que muitas vezes se resolvem sozinhas ou são de origem viral.
Da mesma forma, a maioria das dores de garganta e infecções torácicas, como a bronquite aguda em pessoas saudáveis, geralmente são causadas por vírus. Prescrever um antibiótico nessas situações não acelera a cura e expõe o paciente a riscos desnecessários. A melhor abordagem nesses casos é focar em aliviar os sintomas e deixar o corpo combater o vírus.
Essa mudança de protocolo visa proteger tanto o paciente quanto a eficácia dos próprios antibióticos a longo prazo. A decisão de usar ou não um antibiótico deve ser sempre baseada em um diagnóstico cuidadoso. Confiar no seu médico é o caminho mais seguro para garantir o tratamento correto para o seu problema.
Os possíveis efeitos colaterais

Apesar de serem medicamentos que salvam vidas, os antibióticos não são isentos de efeitos colaterais. É importante estar ciente de que, ao tomá-los, algumas reações adversas podem ocorrer. Felizmente, na maioria dos casos, esses efeitos são leves e temporários.
Os sintomas mais comuns incluem problemas digestivos como diarreia, náuseas e dor de estômago. Isso ocorre porque os antibióticos podem afetar as bactérias benéficas que vivem em nosso intestino. Outros efeitos podem ser tonturas, erupções cutâneas ou o surgimento de infecções fúngicas, como a candidíase.
A boa notícia é que esses efeitos secundários geralmente desaparecem assim que você termina o tratamento. Se os sintomas forem muito incômodos, é sempre importante conversar com seu médico. Ele poderá orientar sobre como minimizar o desconforto ou, se necessário, ajustar a medicação.
Reações alérgicas a antibióticos
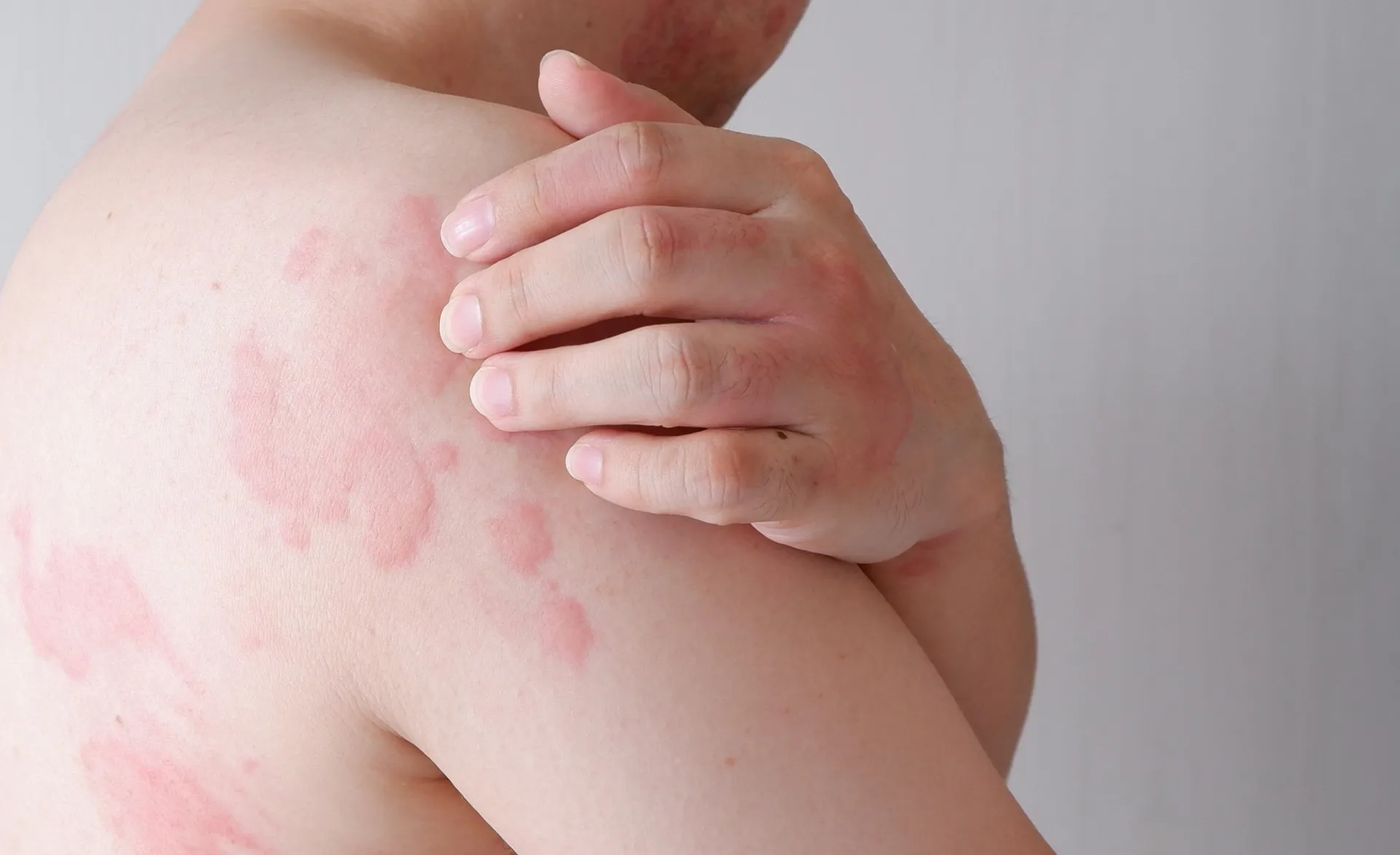
Embora raro, algumas pessoas podem desenvolver uma reação alérgica a certos antibióticos, sendo a penicilina a mais conhecida por isso. Uma alergia é uma resposta exagerada do sistema imunológico ao medicamento, que ele passa a ver como uma ameaça. É crucial saber identificar os sinais de uma reação alérgica.
Os sintomas podem variar de leves a graves, incluindo uma erupção cutânea elevada conhecida como urticária, inchaço da língua ou do rosto e coceira intensa. Em casos mais sérios, podem ocorrer tosse, chiado no peito e dificuldade para respirar. Estes últimos são sinais de anafilaxia, uma emergência médica que requer atenção imediata.
É fundamental que você sempre informe seu médico se suspeita que tem alergia a algum antibiótico ou se já teve uma reação no passado. Essa informação é vital para que ele possa prescrever um medicamento seguro para você. A segurança do paciente vem sempre em primeiro lugar.
Resistência a antibióticos: Uma ameaça crescente

Estamos diante de um dos maiores desafios de saúde pública do nosso tempo: a resistência a antibióticos. Esse fenômeno perigoso é causado principalmente pelo uso excessivo e inadequado desses medicamentos ao longo das décadas. A cada vez que usamos um antibiótico de forma incorreta, damos às bactérias uma chance de aprender a se defender.
A resistência aos antibióticos ocorre quando as bactérias sofrem mutações e se modificam em resposta ao uso dos medicamentos. É importante entender um ponto crucial: são as bactérias que se tornam resistentes, não os seres humanos. Elas desenvolvem mecanismos de defesa que tornam os antibióticos ineficazes contra elas.
Esse processo de seleção natural acelerado está criando “superbactérias” que são imunes a múltiplos tipos de antibióticos. Estamos, aos poucos, perdendo as ferramentas que nos protegeram por quase um século. Reverter essa tendência exige um esforço global e uma mudança de comportamento de todos nós.
Como as bactérias se tornam resistentes
A resistência bacteriana é um exemplo fascinante e assustador da evolução em ação. Quando uma população de bactérias é exposta a um antibiótico, a maioria delas morre, mas algumas poucas podem sobreviver. Essas sobreviventes geralmente possuem alguma característica genética aleatória que as torna menos vulneráveis ao medicamento.
Essas bactérias resistentes, agora livres da concorrência, começam a se multiplicar rapidamente, passando seus genes de resistência para as próximas gerações. Em pouco tempo, toda a população de bactérias se torna resistente àquele antibiótico específico. É a sobrevivência do mais apto acontecendo em velocidade máxima dentro do nosso corpo.
Pior ainda, as bactérias podem trocar informações genéticas entre si, espalhando os genes de resistência como se fossem figurinhas. Isso significa que uma bactéria pode se tornar resistente a um antibiótico que ela nunca encontrou antes. É uma rede de defesa microbiana que está se tornando cada vez mais forte e perigosa.
Infecções mais difíceis de tratar

A consequência direta da resistência é que as infecções se tornam muito mais difíceis, e às vezes impossíveis, de tratar. As bactérias resistentes podem infectar os seres humanos da mesma forma que as não resistentes. O grande problema começa quando tentamos combatê-las com os medicamentos habituais.
As infecções causadas por essas superbactérias não respondem aos tratamentos padrão, exigindo antibióticos mais fortes e caros. Muitas vezes, esses medicamentos de “último recurso” também têm mais efeitos colaterais. O tratamento se torna uma corrida contra o tempo para encontrar uma arma que ainda funcione.
Isso representa um retrocesso a uma era pré-antibióticos, onde uma simples infecção poderia se tornar fatal. Procedimentos médicos que hoje consideramos seguros, como cirurgias e quimioterapia, se tornam extremamente arriscados. A ameaça da resistência bacteriana coloca em xeque muitos dos avanços da medicina moderna.
O impacto global da resistência bacteriana
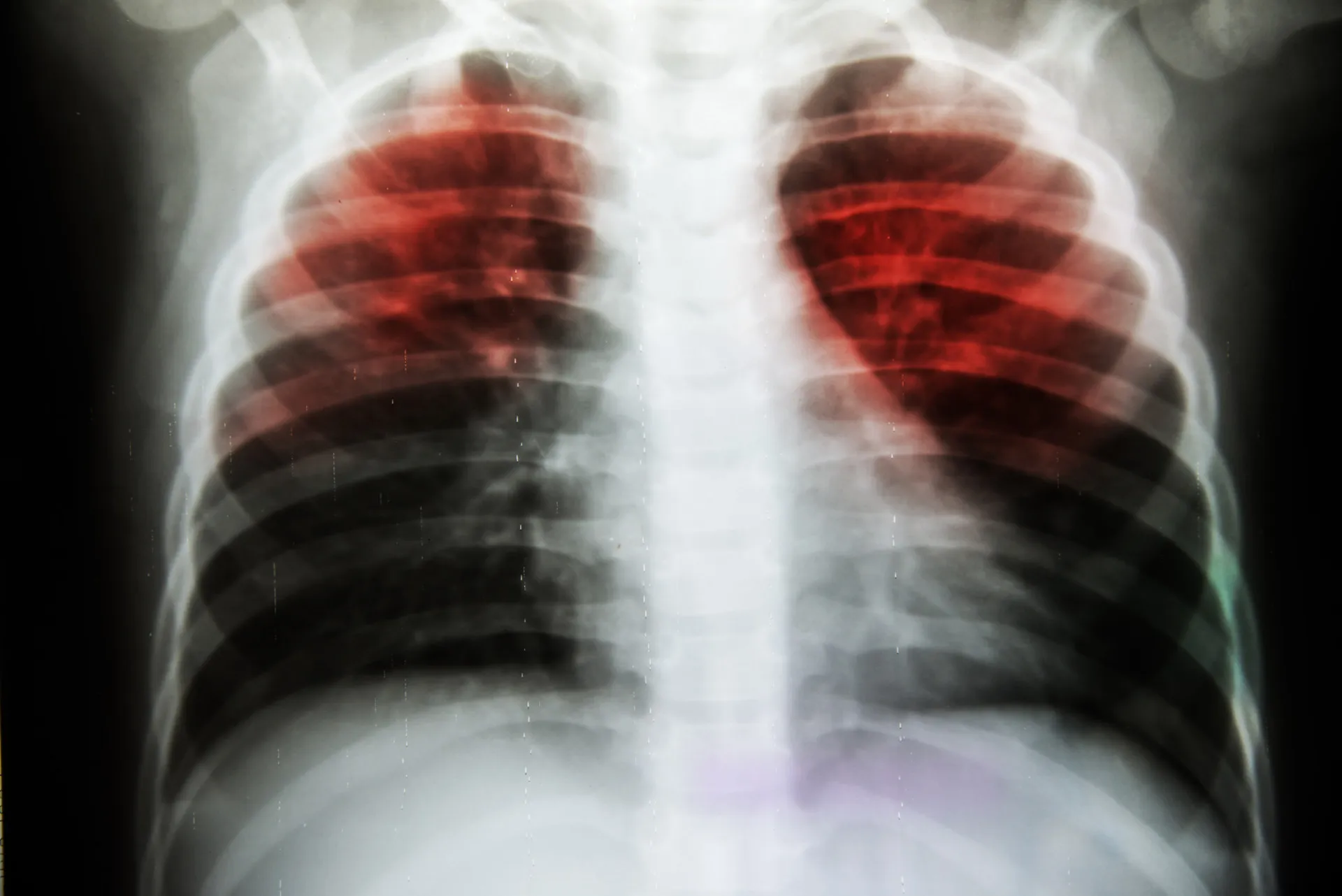
A Organização Mundial da Saúde (OMS) tem soado o alarme sobre a resistência aos antibióticos há anos, classificando-a como uma das maiores ameaças à saúde global. Um número crescente de infecções graves está se tornando cada vez mais difícil de tratar. Isso afeta pessoas em todos os cantos do planeta, independentemente de idade ou condição social.
Doenças como pneumonia, tuberculose, gonorreia e salmonelose estão na lista de preocupações. Os antibióticos que antes eram altamente eficazes para combatê-las estão perdendo seu poder. Isso significa que os tratamentos se tornam mais longos, mais complexos e menos eficazes.
Essa crise não ameaça apenas a saúde individual, mas também a segurança alimentar e o desenvolvimento global. Se não agirmos agora, corremos o risco de ver os grandes avanços médicos do último século serem desfeitos. A luta contra a resistência bacteriana é uma responsabilidade compartilhada por todos.
Custos mais altos e maior mortalidade

As consequências da resistência aos antibióticos vão muito além da dificuldade de tratamento, impactando diretamente os sistemas de saúde e a vida das pessoas. A OMS alerta que o resultado inevitável é um aumento no número de internações hospitalares. Pacientes com infecções resistentes precisam de cuidados mais intensivos e por um período muito maior.
Isso, por sua vez, leva a um aumento drástico nos custos médicos, sobrecarregando os sistemas de saúde e os orçamentos familiares. Tratamentos de segunda ou terceira linha são significativamente mais caros e nem sempre estão disponíveis em todos os lugares. A saúde se torna um luxo que nem todos podem pagar.
Em última análise, o resultado mais trágico é o aumento da mortalidade, pois muitas infecções simplesmente não podem mais ser curadas. Pessoas estão morrendo de doenças que eram facilmente tratáveis há apenas algumas décadas. É um preço muito alto a pagar pelo uso inadequado de um recurso tão precioso.
Estatísticas alarmantes e a busca por esperança
Os números relacionados à resistência bacteriana são sóbrios e revelam a urgência da situação. De acordo com o Centro de Controle e Prevenção de Doenças dos Estados Unidos, o CDC, cerca de 23.000 americanos morrem a cada ano devido a infecções resistentes. Esse número é apenas a ponta do iceberg de um problema global.
Essas mortes são causadas por pelo menos 17 tipos diferentes de infecções que se tornaram resistentes aos antibióticos tradicionais. No entanto, em meio a essa estatística sombria, há uma luz de esperança no horizonte. A comunidade científica está em uma corrida frenética para desenvolver uma nova geração de medicamentos.
Pesquisadores de todo o mundo esperam que novos superantibióticos possam ajudar a reverter essa tendência e reduzir esses números alarmantes. A inovação é nossa melhor arma nessa batalha contínua contra as bactérias. A ciência que nos deu os antibióticos é a mesma que agora busca soluções para preservá-los.
Vancomicina 3.0: A nova geração de superantibióticos

Um dos antibióticos mais potentes que temos atualmente em nosso arsenal é a vancomicina, em uso desde 1958. Ela é frequentemente considerada um medicamento de último recurso, usado quando outros antibióticos falham. No entanto, até mesmo a vancomicina está começando a enfrentar bactérias resistentes.
Mas a ciência não para, e uma nova esperança está surgindo na forma de um superantibiótico chamado Vancomicina 3.0. Pesquisadores conseguiram modificar a molécula original, tornando-a incrivelmente mais poderosa. Estima-se que essa nova versão seja 25 mil vezes mais potente que seus antecessores.
Atualmente, a Vancomicina 3.0 está passando por rigorosos testes clínicos, conforme relatado na revista científica *Proceedings of the National Academy of Sciences*. Se aprovada, ela poderá representar um avanço monumental no tratamento de infecções perigosas. É a inovação científica respondendo diretamente à ameaça da resistência.
A batalha sem fim contra as infecções

A luta contra as infecções bacterianas é uma batalha que nunca terá um fim definitivo, mas que podemos continuar a vencer. Se a Vancomicina 3.0 receber luz verde para uso clínico, nossa capacidade de defesa será enormemente fortalecida. Os químicos que trabalham no Instituto de Pesquisa Scripps, na Califórnia, estão otimistas com o potencial do novo medicamento.
Eles acreditam que essa última linha de defesa contra as infecções mais perigosas se tornará significativamente mais forte e resiliente. Isso nos dará mais tempo e novas ferramentas para combater as superbactérias que ameaçam a saúde global. É um passo crucial para garantir que a medicina moderna continue a proteger vidas.
A jornada dos antibióticos, do pão mofado no Egito aos superantibióticos do futuro, é um testemunho da engenhosidade humana. Ela também nos lembra da importância de usar esses presentes da ciência com sabedoria e respeito. A batalha continua, e a inovação, juntamente com o uso responsável, será a chave para nossa vitória contínua.
